Actualités
Lutte contre la dengue : des alternatives aux OGM
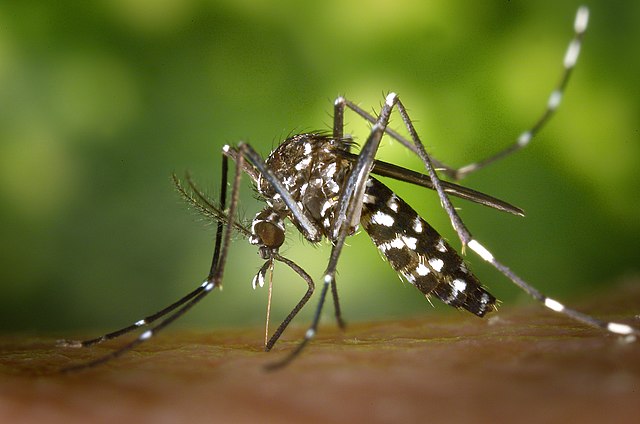
Oxitec, entreprise britannique liée à Syngenta, a obtenu en 2014 l’autorisation commerciale de lâcher dans l’environnement des millions de moustiques génétiquement modifiés pour être « stériles » et ainsi tenter de réduire les populations du moustique Aedes aegypti au-dessous d’un seuil critique pour la transmission de la dengue. Une autre possibilité pour lutter contre la dengue, actuellement en cours d’expérimentation en Australie, au Viêt Nam, en Indonésie, et récemment au Brésil, serait le moustique « immunisé » comme le présentent ses concepteurs de la Fondation Oswaldo Cruz (Cruzeiro) basée à Rio de Janeiro. Comment fonctionne ce nouveau moustique ? Quelles différences par rapport aux moustiques transgéniques ?

Wolbachia est une bactérie qui vit en symbiose à l’intérieur des cellules de certains insectes, elle est pour cette raison dite « endosymbiotique ». Plusieurs techniques mobilisant cette bactérie existent (cf. encadré ci-dessous). La stratégie mise au point en Australie par Scott O’Neill, et actuellement développée au Brésil, consiste dans un premier temps à infecter artificiellement Aedes aegypti par une bactérie Wolbachia provenant d’une autre espèce. Concrètement, les chercheurs ont utilisé le cytoplasme (qui contient les Wolbachia) des œufs de drosophile qu’ils ont injecté dans des œufs d’Aedes aegypti. Pablo Tortosa, chercheur au Centre de Recherche et de Veille sur les Maladies Émergentes dans l’Océan Indien, de l’Université de La Réunion, nous précise que « c’est ce qui est classiquement fait chez les mouches drosophiles mais également plus récemment chez les moustiques tels que Aedes aegypti ou le moustique tigre Aedes albopictus » [1]. Les bactéries Wolbachia sont présentes dans environ 70 % des espèces d’insectes et possèdent deux propriétés d’intérêt majeur quand il s’agit de lutter contre des vecteurs de maladies : elles manipulent la reproduction de leur hôte en augmentant leur caractère invasif d’une part, et rendent, d’autre part, les moustiques artificiellement infectés réfractaires à d’autres parasites tels que le virus de la Dengue. L’équipe de Scott O’Neill a ainsi pu montrer qu’il était relativement aisé de remplacer une population d’Aedes aegypti naturellement non infectée par Wolbachia, par une population de moustiques artificiellement infectée par Wolbachia et par conséquent incapables d’assurer une transmission efficace du virus de la Dengue à l’homme [2].
Substitution de la population locale de moustiques
Après avoir obtenu l’accord de l’Institut brésilien en charge de l’Environnement (IBAMA), la Fondation Oswaldo Cruz (Cruzeiro) basée à Rio de Janeiro a importé des œufs de moustiques vaccinés de l’équipe du Pr O’Neill. Ce projet, qui a fêté ses quatre ans, a déjà mobilisé 1,26 millions de dollars [3]. Le 2 octobre, Fiocruz, une autre fondation publique « à but non lucratif », annonçait avoir lâché 10 000 de leurs moustiques dans un des quartiers nord de Rio, Tubiacanga. Ces lâchers se reproduiront chaque semaine et cela pendant trois ou quatre mois, afin de remplacer la population locale de moustiques par une population infectée par Wolbachia et donc réfractaire au virus de la Dengue, comme cela a été réalisé en Australie. Comme nous le précise Christophe Boëte, chercheur à l’Institut de Recherche pour le Développement (IRD, Montpellier) « la stratégie Wolbachia a été développée mais aussi testée de manière transparente en Australie dans la ville même où les recherches ont été conduites. C’est une très grosse différence avec les moustiques transgéniques développés au Royaume-Uni et testés en premier lieu de manière secrète aux Iles Caïmans ».
Certains habitants dénoncent le fait d’avoir choisi une zone particulièrement pauvre. Pour eux, en cas d’échec, les habitants n’auront pas les moyens de se défendre. La fondation répond qu’il s’agit surtout d’un lieu où la dengue sévit toute l’année.
Interrogé par Inf’OGM, Yvon Perrin, à l’IRD et au Centre National d’Expertise sur les Vecteurs (CNEV), nous précise que l’expérience australienne est prometteuse : « Les premiers résultats de terrain semblent montrer que la bactérie diffuse bien dans les populations naturelles. Il est toutefois difficile d’évaluer l’impact épidémiologique, étant donné que la dengue circule très peu en Australie. Cependant, au laboratoire, le virus est bien « bloqué » dans les femelles porteuses de cette bactérie ».
De même, Luciano Moreira, responsable de ce projet au Brésil, reconnaît que l’efficacité de cette technique ne sera pas connue avant plusieurs années. Si, confiant, il suggère que cette immunité pourrait aussi être efficace, à 60 %, contre la fièvre jaune ou le chikungunya, prudent, il précise qu’il ne s’agit que d’une projection… On est loin du discours fanfaronnant et triomphaliste d’Oxitec…
Une alternative moins chère (et plus sûre ?) que le moustique GM
Contrairement à la stratégie d’Oxitec, qui impose des lâchers réguliers et en masse pour maintenir une certaine forme d’efficacité, cette stratégie semble plus légère. Mais son efficacité est, pour d’autres raisons, questionnée. Les chercheurs reconnaissent que le virus de la Dengue peut évoluer génétiquement, ce qui limiterait l’efficacité de cette méthode. Cependant, pour Luciano Moreira, cette évolution sera lente, ce qui permet de réduire de fait l’ampleur de l’épidémie « pendant des décennies ». Pour Pablo Tortosa, de l’Université de la Réunion, « la stratégie est clairement séduisante même si on ne sait pas si le virus de la dengue va pouvoir s’adapter à ces nouvelles populations d’Aedes aegypti infectées et contourner la barrière Wolbachia, et surtout il est difficile de préjuger de la virulence d’un tel virus adapté » [4].
Yvon Perrin nous précise que, pour lui, « le principal risque serait qu’en rendant la population de moustiques réfractaire à l’infection par le virus de la dengue, ces mêmes moustiques pourraient devenir plus compétents pour transmettre d’autres agents pathogènes (chikungunya, zika, Ross River, ou autres), ce qui a déjà été montré pour une autre espèce de moustique [5] ».
Et de continuer : « De manière plus anecdotique mais pas négligeable, cette technique ne réduit pas les densités de moustique (donc la nuisance), ce qui peut limiter l’acceptation par le public ». Mais ceci peut aussi être un facteur de réduction de risque. Christophe Boëte nous affirme en effet que « contrairement à la stratégie transgénique, cette dernière ne vise pas à supprimer une population d’insectes vecteurs mais à les remplacer par des non-vecteurs, la niche écologique ne devient donc pas ’vacante’ ». On se souvient qu’une des critiques était que la « disparition possible » d’Aedes aegypti pourrait permettre à d’autres moustiques de se développer, comme le moustique tigre.
Quant au biologiste Rafael Freitas, qui travaille dans le laboratoire de la Fiocruz, il considère cette méthode comme « sûre« , car la bactérie Wolbachia n’est pas nuisible à l’homme.
Concernant le coût de cette technologie, Yvon Perrin estime que le lâcher de moustiques réfractaires à la dengue « pourrait effectivement être moins cher que la technique développée par Oxitec, étant donné que la bactérie diffuse d’elle-même dans les populations naturelles, ce qui limite le nombre de lâchers nécessaires » [6]. Ce que confirme Christophe Boëte : « les Wolbachia sont censées se propager d’elles-mêmes ce qui ne contraint pas à faire des lâchers répétitifs comme ce devrait certainement être le cas avec les moustiques transgéniques. On a une solution qui semble donc plus ’durable’ ».
Et si on envisageait une alternative à l’alternative ?
L’équipe de Pablo Tortosa, elle, travaille sur une autre voie, à mi-distance de la solution Oxitec et de celle actuellement testée par Fiocruz, et finalement assez proche de la technique dite de l’insecte stérile consistant à lâcher de grandes quantités de mâles stériles qui vont venir spécifiquement stériliser les femelles sauvages et ainsi maintenir les populations naturelles à des niveaux extrêmement bas, bloquant alors la transmission de virus tels que la dengue ou le chikungunya. Il s’agit de produire en masse des mâles incompatibles (ou stérilisants) et de les lâcher dans la nature en utilisant, encore une fois la bactérie Wolbachia. En fonction de la souche utilisée (cf. encadré ci-dessous), cette bactérie peut conférer une incompatibilité cytoplasmique, c’est-à-dire une forme de stérilité qui selon l’équipe réunionnaise est totale, contrairement à la stérilité obtenue par transgenèse d’après les documents internes d’Oxitec. Pour le chercheur, « cette stratégie est plus lourde que celle de Fiocruz car elle nécessite de produire des mâles en masse et de les relâcher de façon plus ou moins continue pour maintenir les populations natives à un niveau faible, mais c’est à mon avis une stratégie moins risquée que la stratégie de remplacement de population pour les raisons évoquées précédemment ». Mais, à nouveau, le chercheur se veut prudent et reconnaît volontiers certaines limites. Actuellement, les laboratoires ont mis au point deux lignées de moustiques incompatibles (une du genre Culex et une autre de l’espèce Aedes albopictus). Mais, reconnaît le chercheur, le verrou technique se situe dans la mise au point d’un outil de sexage efficace. En effet pour que cette stratégie fonctionne, il ne faut relâcher que des mâles, et en grand nombre.
La même contrainte existe dans le cadre du projet d’Oxitec ou de l’irradiation des moustiques mise en œuvre dans la technique de l’insecte stérile. C’est donc la raison pour laquelle l’Agence internationale de l’Énergie Atomique (AIEA), qui promeut la stratégie « irradiation » dans la lutte contre la dengue, a accordé au laboratoire de l’Université de la Réunion un financement pour développer un outil de sexage qu’elle pourrait réutiliser. Selon Pablo Tortosa, l’entreprise Oxitec a également développé un outil de sexage (qui consiste à produire des femelles dépourvues d’ailes [7]) mais, nous confie-t-il, « ils sont assez avares en infos et une collègue brésilienne qui lâche les mâles Aegypti d’Oxitec au Brésil continue à ce jour à séparer les mâles et les femelles par des méthodes mécaniques ».
A écouter ces chercheurs, la solution Wolbachia semble une alternative pertinente à la solution transgénique. Non seulement il s’agit d’une recherche publique, menée dans la transparence, mais elle aurait un coût inférieur, du fait d’un nombre de lâchers nécessaires moins important, elle n’est pas protégée par des droits de propriété intellectuelle et la bactérie Wolbachia, présente naturellement chez des millions d’insectes, ne semble pas nocive pour l’homme… Que d’avantages !
La technique seule ne remplacera jamais une bonne politique de santé publique
Mais, malgré ces nombreux avantages, gardons à l’esprit qu’il s’agit là encore d’une solution technique. Or, comme le rappelle Christophe Boëte, interrogé par Inf’OGM, quelle que soit la stratégie adoptée, transgenèse, Wolbachia ou irradiation, « ces technologies tendent à faire ’reposer’ les approches de santé publique sur le moustiques et à diminuer l’implication de l’humain. C’est aussi une approche reposant sur une vision d’un progrès technique et technologique porteur de solutions qui tendent souvent à faire l’impasse sur une approche plus globale des problèmes de santé publique ». L’approche technologique non seulement mobilise des ressources, qui sont limitées, et demande une bonne communication entre les scientifiques et le public concerné [8]… mais aussi, et surtout, modifie l’approche sanitaire de l’épidémie : « Avec les stratégies de lutte contre l’épidémie avec des moustiques GM, le pouvoir n’est plus entre les mains du personnel soignant, ni des personnes affectées par la maladie, mais il est concentré dans le corps du moustique lui-même. Le moustique GM devient un outil volant de contrôle sanitaire. Ceci rend la technique particulièrement sensible aux effets imprévisibles et incertains de la mutation biologique [9] »… La technique a besoin d’être comprise et intégrée dans une politique globale de réduction des risques… Elle ne pourra pas se substituer à elle, ce qu’elle tend irrémédiablement à faire.
Comment introduire la bactérie Wolbachia dans le moustique ?
Explications de Pablo Tortosa, chercheur à l’Université de la Réunion :
L’introduction d’une bactérie Wolbachia ne passe pas obligatoirement par l’injection.
A l’instar de Célestine Atyame [10], qui a travaillé avec le moustique Culex quinquefasciatus, on peut introduire une Wolbachia provenant d’une population naturelle de moustique vers une lignée d’élevage de la même espèce de moustique par simple croisement. Ceci présuppose qu’il existe, dans les populations naturelles, des Wolbachia suffisamment différentes entre les populations pour induire une stérilité (appelée Incompatibilité Cytoplasmique ou IC) entre populations.
Ou comme l’a réalisé l’équipe de Stephen Dobson chez Aedes polynesiensis, on peut aussi introduire une Wolbachia d’une espèce A de moustique vers une espèce B de moustique lorsque les deux espèces sont suffisamment proches pour être croisées (on force ces croisements [11]).
Chez le moustique tigre Aedes albopictus, en revanche, à ce jour une incompatibilité cytoplasmique forte n’a pu être obtenue que par injection artificielle (Calvitti et al.).
Wolbachia : une bactérie aux multiples effets
Il existe de nombreuses souches de Wolbachia. Toutes ne produisent pas les mêmes effets quand elles sont présentes dans l’organisme d’un insecte. Ainsi, la souche wMel, par exemple, présente nativement chez la Drosophila melanogaster, et inoculée avec succès chez Aedes aegypti, induit une incompatibilité cytoplasmique (une stérilité) et rentre en interférence avec le virus de la dengue. La souche wRi, présente chez Drosophila simulans, n’induit chez le moustique Aedes qu’une incompatibilité cytoplasmique. D’autres souches telle qu’une souche isolée à partir de drosophiles, appelée pop-corn car elle se multiplie à des niveaux extrêmement élevés chez les moustiques, peuvent conduire à une réduction de la fécondité ou de la durée de vie des adultes ce qui pourrait être avantageux dans le contrôle de la transmission du paludisme dont on sait qu’il met essentiellement en jeu des femelles âgées, qui seraient éradiquées par l’infection pop-corn…
Chine – âcher des millions de moustiques innoculés par Wolbachia bientôt lâchés
A Ghangshou (Canton), dans le sud est de la Chine, la « plus grosse fabrique du moustique du monde » a été construite sur 3500 m2 [12]. Elle prétend produire 20 millions de moustiques Aedes albopictus inoculés avec la bactérie Wolbachia, hebdomadairement. A l’heure actuelle, un premier lâcher de 500 000 moustiques mâles a été réalisé sur une petite île au large de la ville, en mars 2015. Selon Xi Zhiyong, responsable de l’expérience, et professeur à l’Université chinoise de Sun Yat-sen et à l’Université de l’état du Michigan, a annoncé qu’en juin 2015, la population de moustique de l’île avait diminué de 50%. L’avantage de cette technique, souligne-t-il aussi, par rapport à la version transgénique est que Wolbachia passe les générations.
Le programme « Eliminate Dengue » [13] – en partie financé par le Bill & Melinda Gates Foundation – précise avoir disséminé des moustiques Aedes aegypti, eux aussi inoculés avec Wolbachia, en Australie, Brésil, Colombie, Indonésie et Viêt-nam.
[6] Selon le chercheur de l’Université de l’état de São Paulo, Jayme Souza-Neto, la solution transgénique pourrait coûter à une ville de 50 000 habitants entre 710 000 et 1,6 million d’euros la première année, puis environ 335 000 euros les années suivantes pour maintenir une population transgénique suffisante pour s’accoupler et stériliser les populations sauvages. Une manne certaine pour Oxitec…
[7] « Flightless mosquitoes may curb dengue : study », Reuters, 22 février 2010
[8] Christophe Boëte nous cite par exemple le cas d’un programme, en Inde, dans les années 70 qui a échoué, pour cette raison : http://www.readcube.com/articles/10.1038/256355a0
[9] Beisel, U. and C. Boëte. 2013. « The Flying Public Health Tool : Genetically Modified Mosquitoes and Malaria Control », Science as Culture, 22:1, 38-60