Actualités
Malgré écueils et dangers, le forçage génétique toujours d’actualité
En septembre 2025, l’Académie des sciences a publié une synthèse des risques qu’elle a identifié comme associés au forçage génétique. Cette technique, apparue il y a une dizaine d’années, présente des dangers potentiels variés et est incontrôlable. De ce fait, elle n’a pas encore été déployée dans la nature. Cependant, le contexte actuel est très propice à son développement et le principe de précaution est menacé.

Inf’OGM a dédié un dossier complet au forçage génétique en 20201. Cinq ans après, le compte-rendu de l’Académie des sciences2 permet de faire le point sur les nouveaux problèmes émergents et de poser les bases d’une réflexion éthique et philosophique.
Par ailleurs, en août de cette même année 2025, le projet de forçage génétique des moustiques vecteurs du paludisme a subi un coup d’arrêt au Burkina Faso. Quelles en sont les raisons ?
Un projet hégémonique basé sur la transgénèse
Rappelons que la technologie du forçage génétique repose sur la transgénèse chez les espèces sexuées. Les fragments d’ADN (ou cassette transgénique) utilisés codent pour le complexe Crispr/Cas, outil qui permettra de couper l’ADN et de copier la cassette transgénique à l’identique dans la cellule issue de la fécondation. Cette cassette peut contenir un ou plusieurs gènes « d’intérêt » si nécessaire3.
L’objectif est que tous les descendants portent le caractère voulu par les techniciens. Ces caractères seront forcés par la technique. Cela se produira à chaque génération et donc, petit à petit, en théorie, tous les descendants seraient génétiquement modifiés avec la cassette de forçage. Cette transmission est hégémonique et sera d’autant plus effective que l’espèce concernée a une durée de vie courte.
Cependant, la mise en œuvre du forçage génétique est très difficile et présente de nombreux risques. Comme le dit le compte rendu de l’Académie des sciences, « il est intrinsèquement difficile de procéder à une évaluation des avantages et des risques du gène CRISPR homing gene drive.4 Il est impossible d’anticiper pleinement tous les impacts possibles. De plus, il n’existe pas de méthode standard permettant de peser le pour et le contre de manière à satisfaire tout le monde, selon leurs différents points de vue ». Ce qui explique que malgré les nombreuses promesses avancées par les bio-techniciens et l’industrie, le forçage génétique n’ait pas encore été déployé dans la nature.
Les promesses du forçage génétique
Les promesses du forçage génétique concernent la santé publique, l’agriculture et la conservation des espèces.
En médecine, le forçage génétique est envisagé dans l’espoir de contrôler ou éliminer les maladies vectorielles en ciblant les organismes porteurs de maladies, en particulier les moustiques, par exemple contre le paludisme (voir encadré).
En agriculture, les promesses concernent la lutte contre les insectes considérés comme nuisibles (mouches des fruits, criquets, etc.) qui endommagent les cultures ou affectent le bétail. Le forçage génétique est étudié pour réintroduire des gènes de sensibilité dans les mauvaises herbes devenues tolérantes à des herbicides pour qu’elles redeviennent sensibles à ces herbicides !
Enfin, dans le domaine de la conservation des espèces, les promesses du forçage génétique concernent la protection des espèces menacées en contrôlant les espèces envahissantes végétales ou animales ou en introduisant des traits bénéfiques chez les populations à risque d’extinction.
Deux approches sont envisagées pour le forçage génétique : la modification et la suppression.
Dans le premier cas, l’objectif est d’obtenir une population dont 100 % des membres sont porteurs de l’élément transgénique de forçage génétique. Dans le second, il est de réduire ou d’éliminer une population cible, par exemple, en introduisant des modifications génétiques qui provoquent une stérilité spécifique au sexe ou qui réduisent le succès reproductif, entraînant l’effondrement de la population.
Une mise en œuvre compliquée
Les difficultés de mise en œuvre sont de deux ordres. D’une part, il existe des limites biologiques qui rendraient le forçage génétique peu ou pas efficace et, d’autre part, des cas où le forçage génétique ne pourrait pas être arrêté.
Les risques d’inefficacité
En laboratoire, des systèmes de forçage génétique ont été mis au point chez des levures et divers animaux à reproduction sexuée, notamment des mouches, des moustiques et des souris. Dans le cas des plantes, l’application du forçage génétique est difficile pour plusieurs raisons. Beaucoup de plantes se reproduisent de façon végétative, ce qui limite la propagation d’un transgène forcé5. Elles ont des cycles de vie longs, beaucoup d’espèces sont polyploïdes6, rendant la technique beaucoup plus difficile à appliquer. Enfin, la réparation des chromosomes suite à leur cassure générée par Crispr/Cas se fait moins bien que chez les animaux.
Chez les insectes, il existe des espèces proches qui sont capables de se reproduire entre elles, mais qui ne le font pas pour des raisons biologiques ou écologiques conduisant à un isolement reproducteur. On les appelle espèces cryptiques. Dans le cas des campagnes de suppression des moustiques vecteurs de pathogènes, l’élimination réussie d’une population ciblée par un transgène forcé pourrait laisser une niche écologique vide, que des espèces cryptiques de moustiques pourraient combler. Cela pourrait donc conduire à l’expansion de ces espèces cryptiques, elles aussi vectrices du pathogène. Dans un tel scénario, le transgène forcé initial échouerait.
Une autre raison potentielle d’échec est la résistance de certaines populations cibles au forçage génétique, soit par le biais d’allèles de résistance déjà présents, soit par le biais de nouvelles mutations. Des stratégies sont actuellement étudiées en laboratoire pour contrer cette résistance, mais on ne peut prévoir ce qu’elles donneront dans les conditions écologiques naturelles.
Les risques de ne pas pouvoir arrêter le forçage génétique
En cas d’effets indésirables suite à la mise en œuvre d’un transgène forcé, on pourrait vouloir l’arrêter. Cependant, arrêter un transgène forcé n’est pas simple puisque la transmission est hégémonique. Un transgène forcé pourrait continuer à se propager au sein de la population ciblée, même si sa mise en œuvre a été arrêtée.
Ainsi, dans les laboratoires, certains chercheurs tentent de mettre en place des stratégies complexes, toujours à base de transgénèse, pour inactiver les gènes codant le système Crispr/Cas. Cependant, ces modèles théoriques dépendent de nombreux facteurs et certains transgènes forcés s’avèrent inarrêtables. Une stratégie envisagée par les techniciens serait de faire synthétiser aux organismes forcés des protéines anti-Crispr découvertes chez les virus bactériophages7. Mais, cette technique appliquée dans la nature demanderait à libérer en continu, sans jamais s’arrêter, des individus forcés et anti-CRISPR !
Malgré ces limites, l’Académie des Sciences en France n’exclut pas pour autant une mise en œuvre du forçage génétique. On peut lire dans son rapport : « d’autres validations expérimentales et modélisations mathématiques, en particulier dans des environnements spatialement hétérogènes, seront nécessaires pour évaluer l’éventail des conditions permettant à cette stratégie anti-drive d’atténuer avec succès la propagation du gène suppressif ». L’auteure de ce rapport ajoute cependant qu’une « surveillance étroite de la population cible et de l’écosystème » sera nécessaire, ce qui implique « que si une première libération de gene drive [forçage génétique] s’avère problématique, les communautés locales sont condamnées à poursuivre des actions de remédiation avec l’équipe de recherche »… Populations locales et chercheurs locaux qui ne sont pas tous d’accord avec les lâchers d’insectes modifiés (voir encadré).
Les dangers des transgènes forcés dans la nature
Le forçage génétique appartient à une catégorie particulière de techniques à fort impact écologique, de même niveau que l’énergie nucléaire et la manipulation de virus8.
Les organismes forcés génétiquement sont conçus pour agir dans des écosystèmes naturels, où de multiples espèces interagissent entre elles et avec leur environnement physique depuis des millions d’années, construisant ainsi un équilibre dynamique, une forme de stabilité9.
Ce que va faire un transgène forcé dans un écosystème où il est entièrement étranger, inconnu et, de surcroît, artificiel est imprévisible. De nombreux types de mutations peuvent se produire dans l’élément de forçage génétique et transformer un forçage original en un nouveau (voir encadré), avec de nouveaux effets indésirables potentiels sur le phénotype des organismes porteurs du forçage et sur les écosystèmes (par exemple, la résistance aux insecticides). De plus, des mutations dans la séquence du transgène d’un des éléments du complexe Crispr/Cas (l’ARN guide) peuvent modifier le site de coupure ciblé dans l’ADN, et la cassette pourra s’insérer ailleurs dans le génome.
Ces impacts écologiques sont relevés par le rapport de l’Académie des Sciences, qui écrit que « l‘élimination d’une espèce envahissante peut avoir pour objectif de rétablir un équilibre ancestral similaire à celui qui existait avant l’invasion. Cependant, l’éradication locale d’une espèce envahissante laisse un vide écologique qui peut déclencher divers effets trophiques en cascade sur la répartition et l’abondance de nombreuses autres espèces en interaction directe et indirecte avec l’espèce éliminée ». L’équilibre ancestral ne peut être rétablit, l’évolution du vivant ne connaît pas la marche arrière, elle instaure à tout moment du nouveau en fonction des contingences. Et c’est bien pourquoi la mise en œuvre du forçage génétique est si difficile et demande à être requestionnée.
Une autre préoccupation majeure est que les transgènes du forçage génétique conçus pour cibler une population spécifique puissent contaminer d’autres populations de la même espèce ou d’une autre espèce. Plus ces transgènes sont présents longtemps dans la nature, plus le risque est grand. Cela peut se faire par reproduction sexuée entre populations ou espèces proches ou par transfert horizontal, principalement par le biais de virus et de micro-organismes capables de transporter des fragments d’ADN. Ce qui est très préoccupant, puisque des espèces éloignées peuvent ainsi être atteintes par le forçage génétique. Un risque pris en compte par l’Académie des Sciences, qui estime que « la probabilité qu’un élément de forçage génétique contamine une autre espèce n’est pas nulle »10.
L’Académie des Sciences demande aux écologues « d’évaluer de manière approfondie le rôle écologique de l’espèce cible au sein de son écosystème ». Tâche plus qu’ardue et peut-être bien impossible de par l’histoire connue du vivant sur Terre. En effet, les « rôles » écologiques des espèces s’imbriquent les uns dans les autres, il n’y en a pas qu’un par espèce et ils se modifient au cours du temps : un écosystème est complexe et évolutif… et notre compréhension des écosystèmes est aussi évolutive !
Les autres risques du forçage génétique
Les risques sociologiques sont pris en compte dans le rapport de l’Académie des sciences. Ils attisent notre curiosité : « Ces risques découlent de la perception du public et des questions de gouvernance. Comme on l’a vu précédemment avec les vaccins contre la COVID-19 pendant la pandémie, une perception négative du public peut se propager rapidement via les réseaux sociaux. L’un des plus grands risques est la dissémination non autorisée d’organismes génétiquement modifiés dans la nature, qu’elle soit accidentelle ou délibérée, car cela pourrait gravement nuire à la confiance du public envers les scientifiques, les institutions ou les régulateurs ». L’ Académie des sciences craint donc que les conséquences du forçage génétique dans la nature nuisent à la réputation des autres biotechnologies, pourtant bien utiles nous dit-elle. Qu’il nous soit permis de penser que, face aux risques majeurs pour l’environnement que constitue le forçage génétique, ce risque « sociologique » est bien minime.
Quant aux populations humaines qui seraient impactées par le forçage génétique, « les scientifiques et les décideurs politiques doivent privilégier la transparence, l’inclusivité et l’engagement actif auprès des populations locales ». Vœu pieux quand on sait que ce sont de grandes entreprises multinationales des pays riches qui veulent introduire dans les pays du « Sud » les moustiques forcés anti-paludisme et que les rencontres avec les populations locales consistent essentiellement à leur faire accepter cette technologie (voir encadré).
La libération accidentelle d’individus génétiquement forcés dans la nature pendant des essais est évoquée dans le compte-rendu et l’auteure en ce domaine nous rassure : les biologistes ont mis en place une série de règles et de protocoles très stricts de sécurité. Cependant, elle ajoute que « les discussions internationales autour de la recherche sur le forçage génétique n’ont pas encore abouti à un ensemble de règles et de lignes directrices à respecter à l’échelle mondiale ».
L’utilisation malveillante du forçage génétique11 est aussi traitée par l’Académie des sciences. Le forçage génétique pourrait servir à construire deux types d’armes biologiques : « des forçages de suppression qui cibleraient les espèces d’insectes nécessaires à l’agriculture (par exemple, à la pollinisation) et des forçages de modification qui rendraient les insectes nuisibles ou vecteurs de maladies résistants aux insecticides ou capables de transmettre des toxines aux humains ». Mais, conclut ce rapport, une mesure préventive efficace serait « d’ exclure des articles scientifiques les détails méthodologiques relatifs à l’application du gène forcé à des espèces non modèles ». Cela semble bien léger au vu de la surveillance généralisée sur le Internet. Ne serait-ce pas plutôt une raison supplémentaire de stopper les recherches sur le forçage génétique ?
Le projet du forçage génétique n’est pas abandonné devant les risques majeurs de destruction des équilibres écologiques. On continue par des méthodes extrêmement sophistiquées à le mettre en place dans les laboratoires, à l’ajuster pour qu’il soit plus efficace, alors qu’on risque de ne pouvoir l’arrêter.
De quel droit des chercheurs et des industriels persistent-il, alors que des solutions écologiques existent pour répondre aux problèmes que veut résoudre le forçage génétique ? Alors que la société dans tous les pays n’a pas été questionnée ? Alors que l’on sait que le vivant est imprévisible et que contrôler les éléments artificiels introduits dans la nature est impossible ?
La réponse est sans doute que les critères de l’industrie dans la balance bénéfices-risques ne sont pas les mêmes que ceux des populations.
Coup d’arrêt au projet de forçage génétique au Burkina Faso
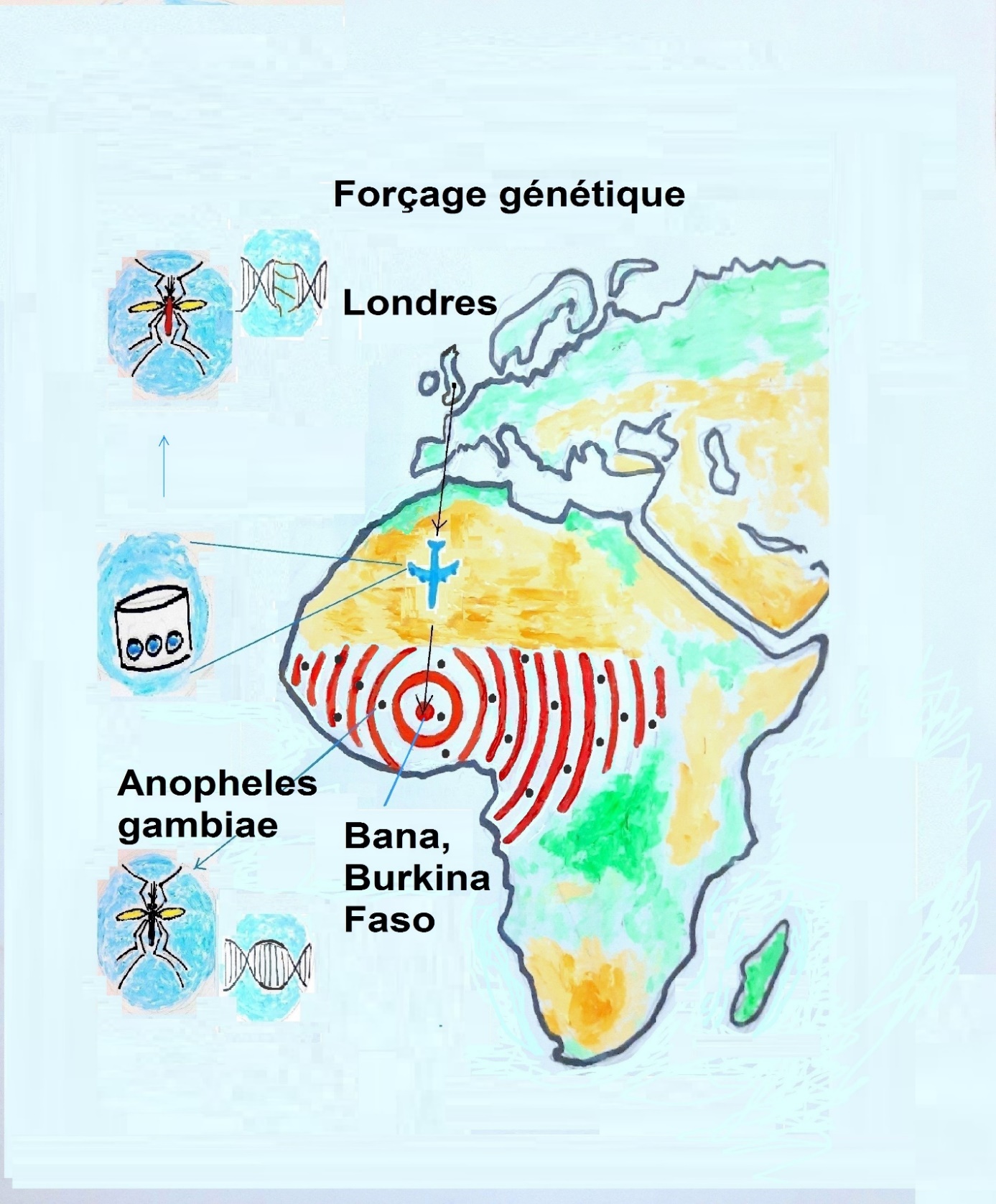
En août 2025, le gouvernement du Burkina Faso a mis fin au projet Target Malaria, qui visait à éradiquer le paludisme en utilisant la technologie du forçage génétique pour éliminer les moustiques Anopheles gambiae, vecteurs de la maladie12.
Ce projet a été conçu dans un laboratoire de l’Imperial College de Londres. Le protocole expérimental du projet comprenait trois phases, chacune centrée sur une souche particulière de moustiques génétiquement modifiés. Seule la troisième phase reposait sur l’utilisation du forçage génétique. Toutes les souches produites par l’Imperial College étaient envoyées à l’équipe locale de Target Malaria au Burkina Faso pour les essais sur le terrain et chaque phase devait normalement se conclure par une libération de moustiques. Ce projet de forçage génétique était le plus avancé au monde, grâce à d’énormes financements, venant principalement de la Fondation Bill et Melinda Gates, mais aussi de la Darpa (Agence étasunienne pour les projets de recherche avancée de défense).
En juillet 2019, lors de la première phase du projet dans le village de Bana, des chercheurs de Target Malaria ont relâché 6 400 moustiques mâles, qui avaient été génétiquement modifiés pour être stériles (mais pas forcés!), afin de voir comment ils allaient s’adapter13. Des irrégularités notoires concernant l’information de la population de Bana avaient été relevées14.
C’est à son stade de deuxième phase, commencée en mars 2022, que le projet vient d’être arrêté. Un lâcher de 16 000 moustiques mâles génétiquement modifiés avait été pratiqué le 11 août 2025. Les moustiques lâchés correspondaient à une autre souche génétiquement modifiée. En fait, les souches de moustiques GM envoyées au Burkina, bien que testées au laboratoire de Londres, ont posé de nombreux problèmes. Andrea Crisanti, qui dirige le laboratoire de Londres, a expliqué lui-même que la souche proposée comportait d’importants défauts susceptibles d’avoir « de multiples implications sur la transmission de la maladie et sur l’adaptation écologique ». Dans la préparation du lâcher, les croisements répétés de la souche génétiquement modifiée avec les moustiques locaux, obligatoires pour assurer son adaptation, auraient mal fonctionné. Andrea Crisanti identifie comme cause l’omission de phénomènes génétiques complexes, comme les inversions chromosomiques, la méconnaissance de gènes liés à la transmission du paludisme ou de ceux liés à l’adaptation à l’humidité ou à la sécheresse. Un autre problème viendrait du fait que les conditions d’élevage des moustiques n’ont pas été maîtrisées sur le terrain, en particulier concernant le degré d’humidité. Les chercheurs et les associations de la société civile qui ont relevé ces défauts ont ainsi permis le retrait du projet15. Ils défendent d’autres méthodes pour lutter contre le paludisme.
D’autres chercheurs de l’Imperial College contestent : « Plusieurs évaluations indépendantes, y compris un examen par l’autorité de réglementation en matière de biosécurité du Burkina Faso et une étude environnementale distincte, ont conclu que les risques liés à la dissémination étaient négligeables »16.
La troisième phase du projet, celle du forçage génétique, en préparation à Londres, est également critiquée. Le rapport d’experts de l’OMS (2022) a identifié des problèmes : la cassette transgénique est devenue instable à cause d’une mutation et le projet ne parvient pas à identifier clairement toutes les espèces de moustiques à cibler17.
1 « Forçage génétique : vers une désorganisation du vivant ? », Inf’OGM, le journal, n°160, juillet/septembre 2020.
« Mini-guide | Forçage génétique : vers un contrôle du vivant ? », Inf’OGM, décembre 2022.
« Forçage génétique : la nouvelle technique qui pourrait éradiquer des espèces entières », Inf’OGM, 18 octobre 2021.
2 Courtier-Orgogozo V., « Risks associated with CRISPR homing gene drive », C R Biol., volume 348, pp. 211-227, 8 septembre 2025.
3 Eric Meunier, « Forçage génétique : une transmission hégémonique de transgène », Inf’OGM, le journal, n°160, Article Inf’OGM, 21 septembre 2020.
4 C’est le nouveau nom donné par les bio-techniciens à la cassette transgénique contenant le complexe Crispr/Cas.
5 L’utilisation de cette expression est une facilité de langage : il s’agit en fait des gènes de la cassette transgénique.
6 Une cellule ou un organisme est polyploïde lorsqu’il possède plus de deux exemplaires d’un même chromosome (exemple : le blé tendre a 7 chromosomes différents avec 6 exemplaires chacun, soit 42 chromosomes).
7 Annick Bossu, « Médecine : les technologies Crispr/Cas se cherchent encore », Inf’OGM, 20 février 2024.
8 C’est le nouveau nom donné par les bio-techniciens à la cassette transgénique contenant le complexe Crispr/Cas.
9 Frédéric Jacquemart, « Biodiversité et stabilité des systèmes naturels : quels impacts des OGM ? », Inf’OGM, 18 novembre 2025.
10 C’est le nouveau nom donné par les bio-techniciens à la cassette transgénique contenant le complexe Crispr/Cas.
11 « Forçage génétique : vers une désorganisation du vivant ? », Inf’OGM, le journal, n°160, juillet/septembre 2020.
12 Abdou Razak OUEDRAOGO, « Santé : Fin des moustiques génétiquement modifiés au Burkina Faso », aconews.net, 22 août 2025.
13 Christophe Noisette, « BURKINA FASO – Les moustiques transgéniques disséminés », Inf’OGM, 3 juillet 2019.
14 Irina Vekcha, « Burkina Faso – Le projet Target Malaria continue malgré les irrégularités », Inf’OGM, 1er février 2022.
15 Irina Vekcha, « Expérimentation du forçage génétique, au Burkina Faso : « Lâcher des moustiques génétiquement modifiés au Burkina Faso est dangereux » estime Mme Irina Vekcha Professeur de génétique à l’ENSA (Université d’Agriculture du Sénégal) », Agropasteur, 4 août 2025.
16 Kai Kupferschmidt, « After ‘humiliating’ raid, Burkina Faso halts ‘gene drive’ project to fight malaria », Science, 3 septembre 2025.
17 Irina Vekcha, « Expérimentation du forçage génétique, au Burkina Faso : « Lâcher des moustiques génétiquement modifiés au Burkina Faso est dangereux » estime Mme Irina Vekcha Professeur de génétique à l’ENSA (Université d’Agriculture du Sénégal) », Agropasteur, 4 août 2025.